
Почти в каждую клетку нашего организма заложен биологический таймер, мерно отсчитывающий время её жизни.
«Известно, что между организмами одного и того же вида существуют различия в длине теломер, например, у человека при рождении выявляются колебания от 5 до 15 тысяч пар нуклеотидных оснований. Однако, точная природа генов, ответственных за установление такого разброса до сих пор не ясна, – поясняет один из авторов исследования Лилия Нигматуллина, младший научный сотрудник OpenLab «Микробные биотехнологии» ИФМиБ КФУ.
Теломерные участки представляют собой своего рода «заглушки» на концах хромосом – плотно упакованных молекул ДНК. Сами «заглушки» состоят из повторяющихся нуклеотидных последовательностей и защищают более значимые области генома. Ещё в 1961 году Леонард Хейфлик наблюдал интересное явление, послужившее основой для теории «молекулярных часов»: в соматических клетках человека после порядка 50 делений запускается механизм клеточного замораживания или самоуничтожения, а при числе делений, приближающихся к пределу Хейфлика, клетки начинают приобретать признаки старения. Теоретическое обоснование эксперимента Хейфлика было получено позднее нашим соотечественником, ныне ведущим научным сотрудником Института биохимической физики РАН А.М. Оловниковым. Выяснилось, что длина теломер уменьшается с каждым последующим делением, что позволяет рассматривать именно этот показатель как наиболее аккуратный клеточный маркер биологического возраста.
В качестве модельного объекта учёными были выбраны растения вида Arabidopsis thaliana, при работе с которыми не возникает проблем с созданием инбредных линий, то есть линий растений, полученных в результате близкородственного скрещивания. Поиск генетических вариаций в человеческом геноме осложнён необходимостью анализа ДНК как минимум у 18000 участников исследования и дополнительным фактом влияния на длину теломер человека не только неблагоприятной генетики, но и его образа жизни.
«На данном этапе проекта мы уже определили гены-регуляторы длины теломер в растениях и сейчас занимаемся изучением механизма работы этих генов, – комментирует Лилия Нигматуллина. – «После нахождения сходных генов у человека мы планируем определить корреляцию между отдельными генетическими мутациями и предрасположенностью к преждевременному старению или к болезням, ассоциированным с ним».
Длину теломер экспериментально измеряли с помощью Southern Blot анализа, сводимого к «нарезке» геномной ДНК растений специальным ферментом, который фрагментирует все последовательности, за исключением теломерной. Далее, в ходе электрофореза теломерной ДНК, последняя распределяется по дорожке используемого геля в зависимости от своего размера, т.е. чем длиннее фрагмент, тем медленнее он двигается по гелю. Следующие этапы анализа связаны с переносом ДНК на нитроцеллюлозный фильтр благодаря капиллярному движению буферного раствора и гибридизацией фиксированной на фильтре ДНК комплементарными нуклеотидными последовательностями, содержащими меченый радионуклид или флуоресцентную метку.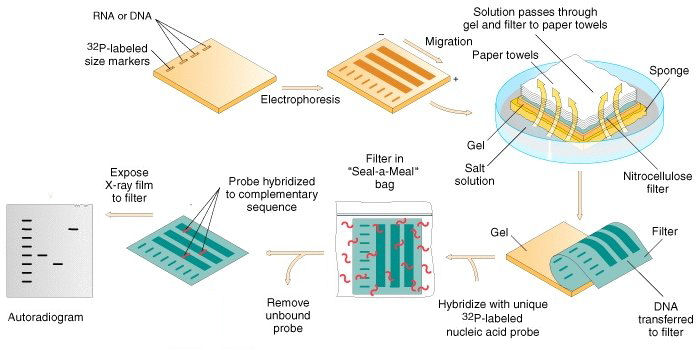 Биоинформационную обработку данных осуществляли с помощью QTL картирования – программы, ищущей корреляции между многочисленными разрозненными признаками.
Биоинформационную обработку данных осуществляли с помощью QTL картирования – программы, ищущей корреляции между многочисленными разрозненными признаками.
«Само по себе старение, конечно же, не исчезнет, поскольку к старению организма приводят и другие факторы. Наша главная цель — поддержание оптимального психического, социального и физического благополучия пожилых людей. В идеале, будем стареть, не болея или болея меньше», — отмечает Лилия Нигматуллина.
*Исследования проводятся под руководством ведущего научного сотрудника ИФМиБ, к.б.н. Шакирова Евгения Витальевича, проект поддержан Инвестиционно-венчурным фондом РТ и Фондом содействия развитию малых форм предприятий в научно-технической сфере в рамках программы «У.М.Н.И.К.»